Nanotecnología contra infecciones intracelulares
Nanopartículas miméticas de linfocitos NK identificaron y destruyeron células infectadas por Staphylococcus aureus
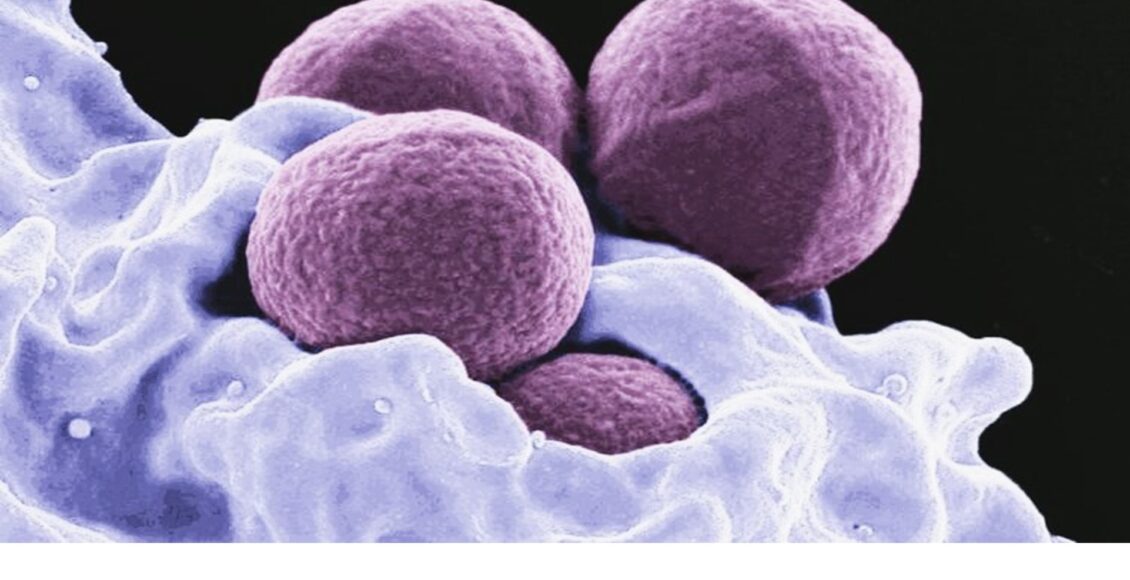
El tratamiento de infecciones causadas por Staphylococcus aureus (S. aureus), especialmente en su forma intracelular y resistente a meticilina o MRSA (methicillin-resistant S. aureus), sigue siendo un gran desafío clínico. Las bacterias que colonizan el interior de osteoblastos y otras células logran evadir tanto a los antibióticos como a los mecanismos inmunitarios, perpetuando infecciones crónicas como la osteomielitis, con una recidiva que puede alcanzar hasta el 40 %.
El estudio de Ge et al., publicado en Science Advances (2024) propone una estrategia innovadora: la creación de nanopartículas miméticas de linfocitos NK o NKMs (natural killer cell mimics), capaces de identificar las células infectadas y erradicar las bacterias intracelulares.
Los investigadores ensayaron NKMs de diseño compuestos de nanopartículas organosílicas mesoporosas dendríticas o DMON (Dendritic Mesoporous Organosilica Nanoparticles) con enlaces disulfuro sensibles al entorno redox celular, carga de perforina y granzima B, dos proteínas clave del arsenal citotóxico natural de las células NK, y modificados con PEG (polyethylene glycol) para darles estabilidad y biocompatibilidad.
En condiciones reductoras, como es el caso de las células infectadas, las DMON se degradan, liberando la perforina que perfora la membrana celular y permite el ingreso de la granzima B, la cual desencadena la muerte del patógeno intracelular. El diseño aprovecha la aumentada actividad redox en osteoblastos infectados por S. aureus como señal de activación selectiva.
Los autores realizaron la validación in vitro mediante modelos celulares MG63 infectados con S. aureus. En esos ensayos, la vancomicina fue incapaz de erradicar las bacterias intracelulares. En cambio, los NKMs fueron altamente eficaces y redujeron significativamente la carga bacteriana, con morfología alterada del S. aureus y daño en la membrana de la célula infectada.
También observaron, por microscopías electrónica y de fuerza atómica, la formación de poros de 10 a 100 nm en las células tratadas. Simulaciones de dinámica molecular confirmaron la interacción perforina–membrana y la formación estable de poros.
Además, se observó una activación del perfil inmunológico de los osteoblastos, con incremento de citocinas proinflamatorias (TNF-α, IL-6, GM-CSF) y rutas relacionadas con la citotoxicidad mediada por células NK.
Para la validación in vivo, usaron un modelo de osteomielitis inducida por implantes en ratones. Los NKMs mostraron una biodistribución favorable y seguridad sistémica, redujeron significativamente la carga bacteriana intracelular y en biopelículas, eliminaron colonias en redes canaliculares osteocíticas, tradicionalmente inaccesibles, superaron en eficacia al tratamiento con rifampicina en alta dosis y promovieron la activación inmune, con mayor proporción de células T CD8+ y NK activadas.
Tras un segundo desafío bacteriano a los tres meses, los animales tratados con NKMs mostraron reducción significativa de carga bacteriana, mayor infiltración de células de memoria T (CD4⁺CD44highCD62Llow y CD8⁺) y reducción de signos histológicos de osteomielitis, lo que sugiere efectos vacunales a largo plazo, por inducción de memoria inmunológica
Este trabajo establece un nuevo paradigma terapéutico: el uso de nanomateriales biomiméticos de células NK para tratar infecciones bacterianas intracelulares, superando las limitaciones de los antibióticos convencionales.
📌 Si bien el trabajoo se enfocó en S. aureus, la plataforma podría adaptarse para tratar otras infecciones intracelulares, como las producidas por Mycobacterium tuberculosis o Salmonella) y avanzar en la frontera entre inmunoterapia e ingeniería de nanomateriales.
